TauroLock® tünelli ve tünelsiz damar kateterleri veya port sistemlerinde tedavi aralarında dahili akış sistemini olumsuz etkileyecek bakteriyel veya fungal biyofilm oluşumlarını önleyici kateter kilit solüsyonudur.
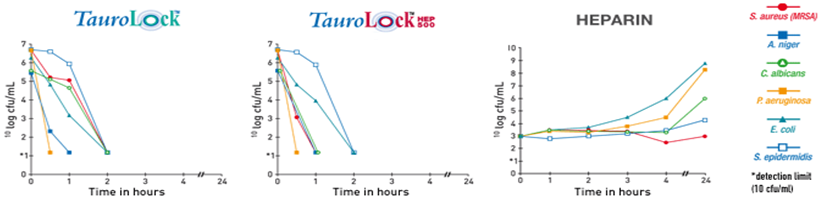
ANTİBİKROBİYAL ETKİNLİK
Kataterle ilgili kan basıncı enfeksiyonlarına karşı korunma:
Merkezi venöz kataterler (CVC) hemodiyaliz, onkoloji, ICU ve toplam parenteral beslenmede kısa veya uzun vadeli vasküler giriş kataterlerde kullanılır. CVC işlevsizliği için büyük riskler, kataterle ilişkili enfeksiyonlardır (CRI). Bu enfeksiyonlar kataterin mikrobiyal kolonizasyonu ile tetiklenebilir ve mikroorganizmalar buradan kan akışına yayılabilir. CRI, kataterin anında çıkartılmasını gerektiren septik semptomlar geliştirebilir.
TauroLockTM kateter kilit solüsyonları, antibiyotik içermez ve hastalıktan korunma amaçlı geliştirilmiştir.
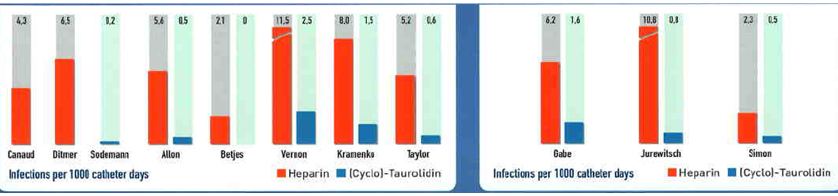
Cyclo-Taurolidine ; Kateterle ilgili enfeksiyonları önemli ölçüde azaltırlar (~%90)
Sitrat (%4) (cyclo)-taurolidine’li ve heparin/ürokinazın birleşiminin de ,MRSA ve VRE gibi dayanıklı mikroorganizmalara karşı mükemmel önlem alan ,bir pıhtılaşma önleyici ve anti-mikrobiyal özelliklere sahiptir.
Bu sebeple, TauroLockTM Alman Diyaliz Standartlarını tamamlayan Hijyen Yönergeleri, Pediyatrik Onkoloji ve Hematoloji Alman Topluluğu’nun (GPOH) kanıtlanmış tavsiyeleri ve Bonn Üniversitesi (Almanya)’nın hijyen yönergeleri gibi farklı yönergelerde (bakınız ref. A) tavsiye edilmiştir.
- TauroLock® daha etkilidir...
- Kalıcı ve geçici kateter kullanan hastalar içindir .
- Kateter lümeninde TauroLock® kullanılması enfeksiyonları önler.
- TauroLock® bakterisidal etkisini birkaç saat içinde gösterir.
- Etkinliği tekrarlayan tüm bakterilerde test edilmiştir.( MRSA ve VRSA dahil).
- TauroLock® un etki alanı bakteri ve mantarların geniş spektrumunu kapsar.
- TauroLock® antibiyotik değildir; bakteriyel direnç gelişmez.
TauroLock® profilaktik olarak kateterlerde planktonik kolonizasyonunu ve biofilm gelişimini önler
- TauroLock Güvenlidir...
- TauroLock Solusyonunda FDA önermeleri gereği %4 sitrat bulunur. Emniyetli ve etkilidir.(Ref: FDA Uyarı Mektubu Nisan 2000)
- Random Enjeksiyon testlerinde yan etki gözlenmemiştir.
- Yüksek nitrat konsantrasyonlu solusyonlarda kalsiyum farklılığından kaynaklanan parmaklarda uyuşma, ağızda metalik tat gibi yan etki riski yoktur. (Ref: 9-10).
- Diğer solusyonlarda yüksek sodyumdan kaynaklanan riskler yoktur.
- Heparin kullanımı ve kalsiyum konsantrasyon farklılıklarından kaynaklanan istenmeyen kanama riski yoktur. Heparin içermez.
- TauroLock® katater lümen yüzeyinde bio-film oluşumunu önler...
- TauroLock® Proflaktik olarak kullanıldığında, kateter lümen yüzeyinde bio-film oluşumunu önler
- TauroLock® bio-film içindeki bakteri ve fungileri inaktive eder, (P. aeruginosa, S. aureus, S. epidermidis, E. faecalis, C. albicans).
- Üst resim : Heparin kilitli kateter: 7 ay implante – S. epidermidis bio-film yüzeyi tamamen kaplamıştır.
- TauroLock® kilitli kateter 5 ay implante: mikrobik kolonizasyon yok.
Taurolock Ürünleri:
- TAUROLOCK (HEPARİN İÇERMEYEN ÖZELLİK) KAT NO: TP-01
- TAUROLOCK HEP 100 (100 UNİT HEPARİN İÇERİR) KAT NO: TP-03
- TAUROLOCK HEP 500 (500 UNİT HEPARİN İÇERİR) KAT NO: TP-02
- TAUROLOCK 25.000 UNIT ÜROKİNAZ KAT NO: TP-05
Kaynaklar :
* Punt, C.D., Boer, W.E. Konsantre trisodyum sitrat enjeksiyonunu takiben kardiyak arrest, Kilnik Nefroloji, 2008, 69: 117-118.
** Willicombe, M.K. Vernon, K., Davenport A., Hipertonik Sitrat Kilit Solüsyonlarıyla Kullanılan Merkezi Venöz Hemodiyaliz Kateterlerinden Embolik Komplikasyonlar, Amerikan Böbrek Hastalıkları Dergisi, 2009, e-pub.
*** Polaschegg, H-D, Sodemann. K. , Kontrantre sitrat içeren kateter kilit solüsyonlarıyla ilgili riskler, Nefrol. Diyal. Translant. 2003, 18:2688-2690.
- TauroLock® nedir?
TauroLock® tünelli ve tünelsiz damar kateterleri veya port sistemlerinde tedavi aralarında dahili akış sistemini olumsuz etkileyecek bakteriyel veya fungal biyofilm oluşumlarını önleyici kateter kilit solüsyonudur.
- TauroLock® 'un etken maddesi nedir?
TauroLock® un bileşiminde tekrarlayan bakteriyel ve fungal enfeksiyonlara karşı antimikrobiyal olarak Cyclo-Taurolidine kullanılmıştır. Cycl-Taurolidine biyofilm oluşumunu da engeller.
- Neden TauroLock® kullanmalıyım?
Amaç, kateterlerdeki ve portlardaki enfeksiyonları önlemektir. Heparin sadece antikoagülan olarak etki ederken bakterileri engellemez. Kateterin sadece bir germ ile kontaminasyonu sebebiyle bakteremiya (kanda geçici bakteri varlığı) sebep olabilir. TauroLock’un koruma amaçlı kullanımı ile biyofilm oluşmasının önlenmesi, kateterin veya portun akışkanlığı artacaktır.
- TauroLock® 'un yan etkileri nelerdir?
Topik veya sistemik etkiler bilinmemektedir. Ürünün hızlı bir şekilde kan dolaşımına enjekte edilmesi durumunda hafif hipokalsemik belirtiler (mesela, metalik tad) meydana gelebilecektir.
- TauroLock® nasıl kullanılır?
1. Aleti 10ml Saline ile yıkayın.
2. Uygun Bir enjektör ile (2,5 ml) TauroLock® ‘u çekin .
3. TauroLock® ‘u kateter lümenine yeterli miktarda doldurunuz. Kateter üreticisinin dolum hacimleri ile ilgili tavsiyelerine uyunuz. TauroLock® Solüsyonu sonraki tedavi uygulamasına kadar kateterde kalacaktır.
4. Yeni tedavi uygulamasından önce , önceki uygulamadan kalan TauroLock® solüsyonu boşaltılmalıdır. - Hastaya TauroLock® enjekte olursa ne olur?
Antimikrobiyel maddenin vücut içerisindeki yarılanma ömrü 30 dakikadan azdır. Doğal olarak ortaya çıkan amino asit taurin içerisine metabolize edilir. Kazara enjeksiyonu sonrasında toksik etkiler beklenmez ve bildirilmemiştir.
- TauroLock® kateterden tahliye edilmez ise ne yapılmalı?
Taurolock yavaşça (yetişkinler: 5 saniyede 1 ml, 3 aydan küçük bebekler : 10 saniyede 1 ml) hastanın kan dolaşımına, herhangi bir risk olmaksızın geçebilir.
- TauroLock® kabul görmüş müdür?
TauroLock® CE-işaretli medikal bir üründür. Tüm avrupa ülkelerinde satılmaktadır.
- TauroLock® hangi miktarlarda satılmaktadır?
TauroLock® 5 ml’lik ampüllerde ve 10 ml’lik flakonlarda bulunmaktatır . Her kutu 10 adet ampül veya 10 adet flakon içermektedir.
- TauroLock® tüm kateterlerde kullanılabilirmi?
TauroLock® farklı poliüretan ve silikon kateterlerde test edilmiştir. Kateter materyallerinde bozunma tespit edilmemiştir.
- Citrat Konsantrasyonu neden sadece %4 tür? Daha iyi bir antikoagülasyon sağlamak için daha yüksek bir konsantrasyon daha iyi olmaz mıydı?
%4 lük bir sitrat konsantrasyonu ABD Federal İlaç İdaresi (FDA) tavsiye edilmektedir. FDA, hastane eczanelerinin ve hemodiyaliz ünitelerinin daha yüksek sitrat içeren bir ürünü (Tricitrasol %46.7) kullanmayı bırakmalarını talep etmiştir . Hollandada, Punt, konsantre (%30) trisodyum sitrat enjeksiyonu sonrasında kalp krizi geçiren iki benzeri vaka bildirmiştir (Punt CD, Boer WE, konsantre trisodyum sitrat enjeksiyonu sonrasında kalp krizi, klinik nefroloji 2008,69 (4), 317-318)
- TauroLock® 'un etkin süresi nasıldır?
TauroLock’un bekleme süresi, heparinin bekleme süresine benzerdir, zira iki maddenin de yoğunlukları birbirine yakındır. Bu, sürekli olarak kan dolaşımına akan yüksek konsantre sitrat çözeltileriyle tezat oluşturur. TauroLock, kateter içerisinde en az 3 ay dengeli olarak kalır.
- Heparin kullanımından TauroLock® kullanımına komplikasyon olmadan geçebilir miyim?
Heparin esaslı Kateter kilit solüsyonu kullanan hastalarda nadir potansiyel problemlere rastlanmıştır.Bu açıdan TauroLock® üreticisi daha önce Heparin kullanılan katerterlerde TauroLock® solusyonu kullanımına geçişlerde kateter ve portlarda 0.5 ml Heparin (5000 Units/ml) ilavesi tavsiye etmektedir. Yeni kateterlerde veya sitratlı kateterlerde bu problem görülmez.
- TauroLock koruyuculu kateteri, laboratuar analizini almak için kullanabilir miyim? (mesela, koagülasyon / pıhtılaşma)
Evet, kullanabilirsiniz. İşlem şöyledir: TauroLock’u aspire ve bertaraf ediniz. Kateteri 10 ml salinle yıkayınız. Kalan sitrat izleri test sonucunu etkilemeyecektir zira koagülasyon testleri için kullanılan test tüpleri %3.13 oranında sitrat içermektedir. Bu yönteme, TauroLock Hep100 veya TauroLock Hep500 kullanılırken izin verilmez.
- Halen, tespit çözeltisi olarak heparin kullanıyorum. Herhangi bir komplikasyon olmaksızın TauroLock'a geçebilir miyim?
Daha önce heparin kullanılarak tespit edilen kateterlere TauroLock tatbiki sonunda bazı durumlarda bloklanmama problemleri bildirilmiştir. Bu sebeple üretici TauroLock’a 0.5 ml heparin (5.000 birim / ml) eklenmesini veya TauroLock – Hep100 (onkoloji, TPN) veya TauroLock – Hep500 (diyaliz) kullanılmasını tavsiye etmektedir.
- TauroLock ve heparinin ön karışımını nasıl önleyebilirim?TauroLock koruyuculu kateteri, laboratuar analizini almak için kullanabilir miyim?
İki adet kullanıma hazır TauroLock çözeltisi mevcuttur, bunlar ek pıhtılaşma önleyici olarak100 IU/mL (TauroLock – Hep100) veya 500 IU/ml heparin (Taurolock Hep500) içermektedir.
- Ne zaman TauroLock™ -Hep100 ve ne zaman TauroLock™ -Hep500 kullanmalıyım?
TauroLock™ -Hep100, çocuk hastalıkları ve onkolojinin tercih ettiği bir üründür. TauroLock™ -Hep500, kritik hastalarda yüksek akımları gerçekleştirmek için diyalizde tercih edilen bir üründür.
FDA Tricitrasolile ilgili uyarılarda bulunuyor. Amerikan gıda ve ilaç yönetimi (FDA) bütün hastane eczanelere hemodiyaliz birimlerine Tricitrasol’un kan yolların açık tutulması amacı kullanımı hasta ölümlerine neden olabilecegi konusunda uyarılarda bulunmaktadır. Tricitrasol 30ml. cam şişeviyolde aynı olarak veya aksesuarları ile birlikte hemodiyaliz kiti olarak satılmaktadır. FDA yakın zaman önce bir hastanın tedavisinde kullanılan 46.7% sodyum sitrat ihtiva eden Tricitrasol enjeksiyonun dan sonra, kalp krizinden ölmüştür. Hızlı ve aşırı sitrat solusyon enjeksiyonu kan kalsiyum kaybına neden olduğundan kalp ritim bozukluğuna neden olabilir ve hatta ölüme sebebiyet verebilir.Tricitrasol’dan kaynaklandığına inanılan diğer bazı vakalarda halen FDA incelemesindedir. Tricitrasol Cytosol Laboratories Braintree.Mass.Firması tarafından üretilmekte ve önceleri Citra Anticoagulantsinc.Simdilerde Medcomp HarleysvillePa. şirketleri tarafından pazarlanmaktadır. Ürün iki şirket tarafından gönüllü olarak piyasadan geri çekilmiştir. FDA ülke çapına hastane eczanelerin ve hemodiyaliz ünitelerine ürünlerin kullanımını durdurmaları konusunda ikaz etmiştir. Alternatif olarak 4% sitrat solusyonları bütün ilgili marketlerde mevcuttur ve kullanımı önerilmektedir. Kantransfüzyonu için gerekli olan akyuvar hazırlığında gerekli bir madde oldugu için FDA ve Firmadilusyon için gereken malzemeyi gözetim altına almıştır. Nisan 2000 yılında Medcomp müşterilerine bir mektup göndererek Tricitrasolitiva eden kitleri ve MedcompAsh Split kateteri, hemodiyaliz, kan ayrıştırma, yeniden transfuzyon kateterlerini geri çağırmıştır. Ülke çapında 3000 Medcomp kiti dağıtılmıştır. Ayrıca Kanada ve Puerto Rico’da dağıtım yapılmıştır. Vakalarla ilgili daha geniş bilgi için Medwatch1-800-FDA-1088 telefonu ile kontak kurabilirsiniz veya email [email protected]
Kullanma Kılavuzu ve Detaylı bilgi için lütfen sayfa sonundaki formu doldurunuz.